Химический «марьяж»
Особенно яркими примерами самоорганизующихся структур располагает современная химия. Все мы знаем, что определенные химические вещества способны вступать друг с другом в реакции, образуя при этом новые вещества. Наиболее, пожалуй, известной такой реакцией является процесс горения, при котором какой-либо элемент (например, углерод) соединяется с кислородом. Эта и подобные ей химические реакции становятся возможны только при определенных условиях; в данном случае это некая минимальная температура, необходимая для возгорания. Химики обнаружили, что существует и другой способ запустить химическую реакцию или, по крайней мере, ускорить ее протекание. Реакция, которая прежде не шла вовсе или шла очень медленно, может быть «поддержана» введением в нее определенных веществ. Такими веществами могут быть металлы — например
пластинка платины; сами они в ходе химической реакции не изменяются, выступая в роли, чем-то похожей на роль свахи: они помогают партнерам соединиться, образовав при этом новое химическое вещество. Эти особые вещества, помогающие вступить в союз другим веществам, называются в химии «катализаторами» (рис. 6.1).
Рис. 6.1. Катализатор в роли химической свахи
В ходе исследований химики столкнулись с явлением, которое поначалу воспринималось ими как некая случайная странность, но со временем приобрело довольно серьезное значение. Дело в том, что существуют химические вещества, которые в состоянии служить катализаторами в реакциях получения самих себя. Звучит это, конечно, довольно запутанно, но означает всего-навсего то, что молекулы такого вещества способны в некотором смысле самостоятельно размножаться. Им удается преобразовывать молекулы других веществ таким образом, что в результате возникают новые молекулы их собственного типа (рис. 6.2).
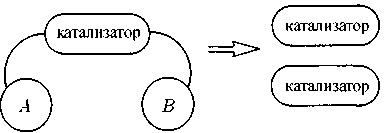
Рис. 6.2. Автокатализ: катализатор соединяет две молекулы таким образом, что получаемые в результате реакции молекулы оказываются идентичны молекуле самого катализатора
В этом процессе уже присутствует нечто, явно схожее по своим свойствам с живой материей, а потому нет ничего удивительного в том, что мы еще столкнемся с этим явлением при рассмотрении теории эволюции. Процессы, подобные описанному, называются автокаталитическими. Что же происходит в ходе химической реакции? При этом нас интересует как микроскопический, так и макроскопический уровень. На микроскопическом уровне вещество состоит из отдельных молекул, а те, в свою очередь, — из атомов. Допустим, некие молекулы двух видов — назовем их вид 1 и вид 2 — вступают в химическую реакцию, в результате которой образуется молекула нового вида (скажем, вида 3). При этом новое вещество может обладать иными химическими и физическими свойствами — например другим цветом. В этом можно легко убедиться, проведя несколько опытов: смешав две жидкости разных цветов — голубую и бесцветную — мы вдруг получаем жидкость красного цвета (рис. 6.3).
Рис. 6.3. Соединение двух различных химических веществ обычно приводит к возникновению гомогенного конечного продукта
Полученная жидкость обычно совершенно равномерно окрашена и не теряет свой цвет со временем. Впрочем, так случается «обычно» — но не всегда; тут мы подбираемся, собственно, к главной теме этой главы. Дело в том, что в XX веке учеными было обнаружено несколько довольно сложных химических реакций, в ходе которых образовывались макроскопические структуры, своими размерами в миллиарды раз превосходящие размеры молекул исходных веществ.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОК